国会活動
2023.3.22 予算委員会「ワクチン死と解剖医が評価それでも認めない不思議」
2023年03月23日
- カテゴリ
○理事(片山さつき君) 次に、山本太郎さんの質疑を行います。山本太郎さん。
○山本太郎君 れいわ新選組代表、山本太郎です。
ワクチンの安全性、個人の救済に関して2つの制度、名前と仕組みの説明を。
○政府参考人(佐原康之君) お答えいたします。
まず、副反応疑い報告制度というものがございます。この制度に基づきまして、新型コロナワクチンの接種を受けたことによるものと疑われる症状につきまして、医師や新型コロナワクチンの製造販売業者等からPMDAを通じて厚生労働省に、厚生労働大臣に報告がされます。この制度は、ワクチン接種後に生じる症状等の傾向を把握することを目的としており、報告された症状の情報については、審議会において、ワクチン接種と副反応疑い事象に関する個別の因果関係の評価や集団としての傾向の評価等を行い、必要な場合には注意喚起を行うなど、安全対策に活用しているところでございます。
もう1つ、予防接種法に基づきます被害救済制度がございます。この制度に基づきまして、ワクチン接種後に健康被害を受けた本人やその家族等が市町村に対して申請を行い、市町村から都道府県を通じて国に対して進達された案件を国の審査会で審査をした上で、予防接種と健康被害との因果関係を認定された方に救済のための給付を行うものでございます。
○山本太郎君 医療機関から来る情報を国としてどう評価していますか。
○政府参考人(八神敦雄君) お答えします。
新型コロナワクチン接種後の副反応疑い事例、これは医療機関、それから企業からもですが、PMDAを通じて厚労省に報告をされております。その際、PMDAは、その選定をした外部専門家の知見を活用して因果関係評価、これを実施をします。それらの個別の評価の、個別事例の評価ですとか必要な情報、これを整理し、併せて提供をし、これを基に定期的に開催をしている審議会において安全性等の評価を行っていると、こういう仕組みでございます。
○山本太郎君 コロナワクチン接種後の死亡、3月10日、評価、そして報告された件数は。
○政府参考人(八神敦雄君) お答えします。
現在接種をされている製薬企業3社の新型コロナワクチンにつきまして、副反応疑い報告制度で報告をされた事例のうち、ワクチン接種後の死亡事例の総数は、本年1月22日時点でございますが、2001件でございます。

○山本太郎君 因果関係が否定できない、何件ですか。
○政府参考人(八神敦雄君) 今申し上げた2001件のうち、ワクチン接種と死亡との因果関係が否定できないと評価された事例は1件でございます。
○山本太郎君 アルファ評価の方のことですね。その方はどんな状況でしたか。
○政府参考人(八神敦雄君) お答え申し上げます。
ワクチン接種直後に症状が発現をし、急激な病状の進行が認められ、ショック、死亡に至った事例でございます。
○山本太郎君 厚労省、コロナワクチンによる副反応が疑われる症状、幾つありますか。
○政府参考人(八神敦雄君) 副反応が疑われる症状というものはないということでございます。数はないということでございます。(発言する者あり)
〔理事片山さつき君退席、委員長着席〕
失礼いたしました。
今お尋ねいただいたのは、報告基準に該当する症例ということでお尋ねいただいたことだとすれば、それは5症状ということでございます。
○山本太郎君 そもそも厚労省が先ほどの副反応の疑いがある症例みたいなものを事前に社会に公表する理由を教えてください。
○政府参考人(佐原康之君) まず一般国民への周知の意義と、それから医療機関への周知の意義とがあると考えております。
一般国民への周知の意義としては、新型コロナワクチンの接種は、生じ得る副反応に関する情報も含め、ワクチンの安全性、有効性に関する正しい情報を基に、本人又は保護者がワクチンを接種すべきかを適切に判断いただくことが重要であると考えております。
次に、医療従事者への周知の意義でございますが、これは、医療機関に対しては、新型コロナワクチンの接種後に副反応が疑われる症状を生じ得ることを、それぞれのワクチンの添付文書における使用上の注意により周知しております。さらに、製造販売業者においても、適正使用ガイドラインといった医療機関向けの説明資料を作成、提供し、副反応に関する情報を提供しております。こうした取組を通じて、副反応の疑いのある症状に対し、医療機関で正しく対処いただくことが重要であると考えております。
○山本太郎君 資料の①。アメリカでは、ファイザー社などがFDAに提出した資料の開示を求めて裁判、開示となった機密資料がホームページで公開。そこには、2021年2月28日までの3か月間で、接種後の死亡報告が1223人、有害事象は42086件、ワクチン接種後に起こり得る1291種類の有害事象のリストが記載されていたと。

これ、自称運び屋、ワクチンといえばやっぱり河野大臣。2021年6月、アメリカで2億回ぐらいコロナウイルスのワクチンを打っているんですけれども、亡くなった人はゼロですと御発言されています。このような公開資料が出てきたことに対してどう思われますか。
○国務大臣(河野太郎君) 当時のアメリカのCDCの資料どおりでございます。
○山本太郎君 改めてこういうものを見てどう思うかという問いだったんですけれども、運び屋は運ぶまでがお仕事ということですかね。
資料の②、議事録。昨年4月、このデータについて、厚労委員会、川田議員から、ファイザーから報告はなかったか、データの存在を知ったのはいつかとの質問に、この質疑で知った、専門家に諮り、その結果を国民の皆様に情報発信したいと考えていると厚労省は答弁。この件、どうなりました。

○政府参考人(八神敦雄君) お答えします。
このファイザーの文書でございますが、ファイザー社に確認をしたところ、ファイザー社より2021年5月にFDAへ提出された承認申請資料の一部であるということ、それから、その中には2021年2月28日までのファイザー社のワクチンの安全性に関する報告が取りまとめられているものというふうに確認をして、承知をしてございます。
この文書そのものは保持をしておりませんけれども、ファイザー社のワクチンの安全性を確認する情報ということで、海外の市販後安全性調査というものを私どもも確認をしておるところでございます。
具体的には、日本におけるワクチンの承認審査において、同社がまとめている当時のマンスリーレポート、これで海外の市販後安全性調査情報について確認をし、また、これは審査報告書にも公表をしているところでございます。また、承認後も、製造販売者である、販売業者であるファイザー社に対して、薬機法に基づき、海外を含む副反応に係る情報を収集し、PMDAに報告することを求めておるところでございます。
なお、新型コロナワクチンの副反応疑い報告の評価におきましては、審議会に対して海外の情報を含め必要な情報を提供をした上で評価をしていただき、その結果、都度ホームページに公表するといった対応をさせていただいているところです。
○山本太郎君 川田さんの質疑で初めて知ったと言っているんですね。で、副反応のこういった情報をいろいろ見ていると言ったけど、1291種類もの有害事象というものがリスト化されていることが分かったわけですよね。
これ、副反応の情報って、医療機関などが万が一のときに現場で対処できるように事前にお知らせをすると先ほどお話ししました、そう答弁ありましたよね。
大臣、じゃ、なぜ、メーカー側から示された1291種類もの有害事象を、これ副反応のリストに加えて医療機関に伝達、社会に報告ということにはならないんでしょうか。
○政府参考人(佐原康之君) 副反応の発生状況につきましては、定期的に審議会において審議をしておりまして、また、その情報については公開をしているところでございます。
また、特に注意すべき副反応につきましては、先ほどの五症状も報告基準という形でお示しをしまして医療機関に注意喚起をしているところでございます。
○山本太郎君 いやいや、メーカー側から、1291種類もの有害事象があるということがリスト化されていて、裁判で開示されたわけでしょう。これ新たに追加していかなくていいんですか、これ。実際にそういうデータが取られたからそういう話になったわけでしょう。日本の専門家に諮ってというよりも、向こう側がそう言っているわけだから、これ追加していくべきじゃないですか。大臣、どう思われます。
○国務大臣(加藤勝信君) 詳細については事務方からお話をさせていただきますが、我が国の場合、基本的には、先ほど、副反応疑いについて審査会についてそれぞれ御議論をいただいて、その内容は透明性を持って開示をさせていただいている、そういった仕組みの中でやらせていただいているところであります。
○山本太郎君 いやいや、国民に広くこれ伝えるということを川田さんの質疑のときに言っているのに、ホームページにちょこっと載せているだけの話でしょう。全然広く広がっていないじゃないですか。しかも、これだけ多くの事象というものに対して、多くの人たち知りませんよ。余りにも不可解ですよ。不透明です。
委員長、政府がファイザー社から取得したコロナワクチン接種後の有害事象報告資料全て、新型コロナワクチンの詳細な安全性に関わる非臨床試験と臨床事件で生じた有害事象の全データ及び新型コロナワクチン購入契約書の本委員会への提出を求めます。
○委員長(末松信介君) 後刻理事会で協議をさせていただきます。
○山本太郎君 資料の④。アルファ評価、それ以外の状況はどうなっていますか。

○政府参考人(八神敦雄君) お答え申し上げます。
死亡例2001件のうちアルファ以外ということで、ワクチンと死亡との因果関係が認められないもの、これは11件、情報不足等によりワクチンと死亡との因果関係が評価できないもの、これが1989件となってございます。
○山本太郎君 つまりは99.4%が評価不能と。
評価不能ってどういう意味ですか。
○政府参考人(八神敦雄君) お答え申し上げます。
情報不足等によりワクチンと死亡との因果関係が評価できないものということで、具体的に2つの場合が考えられます。死因と考えられる事象の判断、事象とワクチンとの因果関係を判断するための情報が不足している場合、また、情報不足ではないが、得られた情報からは、偶発的に起こったもの、合併症によるもの、併用薬によるものなどとの区別ができないものと、こういった2つの例に分かれるということでございます。
○山本太郎君 報告医師がワクチンと死亡が関係ありとしたもの、何件あります。
○政府参考人(八神敦雄君) お答え申し上げます。
死亡例2001件のうち、報告医等から関連ありと報告をされたものは277件報告をされております。
○山本太郎君 厚労省がよく分からないと言っていることが、現場で対処した医師たちは277件因果関係ありですと言っているわけですね。
現場で評価した担当医、病理医の評価を認めない理由何ですか。具体例挙げて説明してください。
○政府参考人(八神敦雄君) お答え申し上げます。
新型コロナワクチン接種後の副反応疑い事例の因果関係の評価に当たりましては、医療機関や製造販売業者から情報を収集、整理、評価をしております。
具体的には、解剖ですとか画像所見等の情報も活用した上で、原疾患との関係、薬理学的な観点や時間的な経過などの要素を勘案し、医学、薬学的観点から総合的に判断をしているところでございますが、ワクチン接種後の症状が偶発的な発生によるものなのか、それともワクチンを原因として発生したものなのかの判断は極めて難しいと考えてございます。
具体例ということでお尋ねございました。不明と、因果関係の評価が、因果関係の評価できないというものの具体的な例ということでございます。例えば、高血圧、こういう既往症がある方、これ以外の情報がなく、医師の調査協力がなかなか得られず情報不足のため死因の特定やワクチンとの因果関係の評価が不能なケースであったり、あるいは、僧帽弁閉鎖不全症及び認知症の基礎疾患があるけれども、ワクチン接種直後は異常がなく、夕食摂取などの後、心肺停止状態となり救急搬送されたが死亡された方、司法解剖されましたが死因が不明でワクチンとの因果関係の評価が不能と、こういったケースがございます。
○山本太郎君 医師が解剖した後に報告したもの、何件あります。うち何件、基準の五症例に当たりましたか。
○政府参考人(八神敦雄君) 副反応疑い報告制度で報告があった死亡事例のうち、解剖が実施された事例というのは230例程度でございます。また、解剖が実施されて報告基準に該当する5症状、これが報告された事例は45例程度報告をされているというところでございます。
○山本太郎君 五症例にないものも含めて、解剖までした医師が52件ワクチンとの関係ありと報告している。医師が解剖した上で因果関係ありとしているのに、それ認めない理由何ですか。現場の解剖で得られていない必要情報って何だったんですか。
○政府参考人(八神敦雄君) 繰り返しになりますけれども、解剖ですとか画像所見等の情報も活用した上で、原疾患との関係、薬理学的な観点や時間的な経過などの要素を勘案し、医学、薬学的観点から総合的に判断をしてございます。ただ、ワクチン接種後の症状が偶発的な発生によるものか、あるいはワクチンを原因として発生したものなのかといった判断は極めて難しいというふうに考えてございます。
○山本太郎君 現場の医師が解剖まで行って因果関係ありと判断したものを、よく分からないという理由で覆すほどのエビデンス、厚労省得られていないのに、よく分からないって横に置いている状態なんですよ。
PMDA審査制度、説明を。
○政府参考人(八神敦雄君) PMDAの業務ということでございますが、PMDAは、PMDAにおける副反応疑い報告に関する業務の流れということで御説明しますが、副反応疑いの事例が医療機関及び企業からPMDAに報告をされ、PMDAが選定をした外部の専門家がその知見を活用して因果関係等の評価を行い、それらの個別事例の評価や必要な情報、これを整理をして審議会に提供をしておると。その後、審議会におきまして安全性の評価が行われるという、こういう段取りでございます。
○山本太郎君 別のワクチンも同じ審査制度ですか。
○政府参考人(八神敦雄君) 同様の仕組みでございます。
○山本太郎君 これまで別のワクチンでの審査結果と対象期間は。
○政府参考人(八神敦雄君) 新型ワクチン、新型コロナワクチンが接種を開始される前に報告された死亡例の評価ということで、例えば令和2年12月の審議会でございますが、令和2年5月1日から令和2年9月30日まで、この期間で23価肺炎球菌ワクチン、この接種後の死亡事例が3件報告をされております。いずれも情報不足のため、ワクチン接種との因果関係は評価できないとされております。
また、令和2年7月及び9月の審議会の例でございますが、2019年から2020年のシーズンのインフルエンザワクチンにおきまして、令和元年10月から令和2年4月30日までの期間で7件の死亡事例が報告をされております。このうち、ワクチン接種との因果関係が認められない旨の評価をされたものが2件、ワクチン接種との因果関係は不明である、又は情報不足のためワクチン接種との因果関係は評価できないと評価されたものが5件というふうに承知をしております。
○山本太郎君 今の答弁が死亡者数多い時期を選んでいるかどうかは分からないんですけど、接種した人数なども異なっているし、単純比較できないという前提で、死亡者数を期間で割り出して1か月の死亡者数として比較すると、コロナワクチンは肺炎球菌ワクチンの約90倍、インフルエンザワクチンの約55倍という、死亡報告事例が多いということになるんですね。
PMDA、収入と内訳教えてください。
○政府参考人(八神敦雄君) お答え申し上げます。
PMDAの総収入額、2019年度ということでお尋ねだったというふうに理解をしております。予算ベースで291.3億円でございます。そのうち、国の予算からの収入は37.8億円、製薬会社からの収入は229.9億円で、割合につきましては、国費分が13%、製薬企業分の民間分は78.3%となっております。
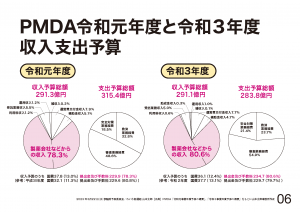
○山本太郎君 因果関係審査する側の毎年の収入、これ、2019年だけじゃなく、7割、8割が審査される側に依存しているんですよ。これでちゃんとしたジャッジできるのかな。
まとめますね。
製薬会社の顔色をうかがうんじゃなくて、厚労省として分からないとするならば、解剖まで行った医師の評価を尊重すること重要じゃないですか。52件解剖を行った、その医師が因果関係ありってしたんですよ。それ覆すんだったら相当の理由が必要になります。そういった現場の人たち、この人たちが行った判断を、分からないと横に置くのではなくて、尊重することが重要だと思います。現在の運用は変えなければならない、そう申し上げて、終わります。
ありがとうございます。
最新の記事
- 2025.12.15 予算委員会「サナエとトランプ 売国棄民、ここに極まれり」
- 2025.12.5 災害対策及び東日本大震災復興特別委員会「「そりゃないですよ!」借金しろでは持たない・・・。八丈島の事業者、経済を救え!」
- 2025.12.2 環境委員会「ウソにウソを重ねたインチキで国民を守る!?」
- 2025.11.26 憲法審査会「憲法改正という詐欺、窃盗行為から国民を守る」
- 2025.11.6 本会議 代表質問
カテゴリ
- PCSC協定
- SPEEDI
- もんじゅ
- グローバー勧告
- サイバー
- テロ関連
- マイナンバー
- ロスジェネ
- 予算委員会
- 健康・医療戦略推進法
- 内閣委員会
- 原子力委員会設置法
- 国家公務員法の一部を改正する法律
- 国家戦略特区法
- 天下り
- 奨学金
- 子宮頸がんワクチン
- 小児甲状腺がん
- 川内原発
- 年次改革要望書
- 放射性物質拡散シミュレーション
- 新型コロナウイルス感染症
- 日米原子力協定
- 東日本大震災復興及び原子力問題特別委員会
- 株式会社地域経済活性化支援機構法の一部を改正する法律
- 水素エネルギー
- 汚染水対策
- 法科大学院
- 特定秘密保護法
- 独立行政法人通則法の一部を改正する法律
- 総合科学技術・イノベーション会議に関する内閣府設置法の一部を改正する法律
- 被ばく問題
- 規制基準
- 重大な犯罪を防止し、及びこれと戦う協力の強化に関する日本国政府とアメリカ合衆国政府との間の協定の実施に関する法律
過去ログ
- 2025年12月
- 2025年11月
- 2025年6月
- 2025年5月
- 2025年4月
- 2025年3月
- 2025年1月
- 2024年12月
- 2024年10月
- 2024年6月
- 2024年5月
- 2024年4月
- 2024年3月
- 2024年2月
- 2024年1月
- 2023年12月
- 2023年11月
- 2023年6月
- 2023年5月
- 2023年4月
- 2023年3月
- 2022年12月
- 2022年11月
- 2022年3月
- 2022年2月
- 2019年6月
- 2019年5月
- 2019年4月
- 2019年3月
- 2019年2月
- 2018年12月
- 2018年11月
- 2018年8月
- 2018年7月
- 2018年6月
- 2018年5月
- 2018年4月
- 2018年3月
- 2018年2月
- 2017年12月
- 2017年8月
- 2017年7月
- 2017年6月
- 2017年5月
- 2017年4月
- 2017年3月
- 2017年2月
- 2017年1月
- 2016年12月
- 2016年11月
- 2016年10月
- 2016年6月
- 2016年5月
- 2016年4月
- 2016年3月
- 2016年2月
- 2016年1月
- 2015年12月
- 2015年10月
- 2015年9月
- 2015年8月
- 2015年7月
- 2015年6月
- 2015年5月
- 2015年4月
- 2015年3月
- 2015年2月
- 2014年11月
- 2014年10月
- 2014年7月
- 2014年6月
- 2014年5月
- 2014年4月
- 2014年3月
- 2013年12月
- 2013年11月
- 2013年7月
- 過去記事一覧







